1. इलेक्ट्रॉनिक विन्यास (Electronic configuration) – लैन्थेनाइडों का सामान्य इलेक्ट्रॉनिक विन्यास [Xe]54 4f1-14 5d0-1 6s2 होता है, जबकि ऐक्टिनाइडों का सामान्य इलेक्ट्रॉनिक विन्यास [Rn]86 5f1-14 6d1-2 7s2 होता है। अतः लैन्थेनाइड 4f श्रेणी से तथा ऐक्टिनाइड 5f श्रेणी से सम्बद्ध होते हैं।
2. ऑक्सीकरण अवस्था (Oxidation states) – लैन्थेनाइड सीमित ऑक्सीकरण अवस्थाएँ (+2, + 3, +4) प्रदर्शित करते हैं जिनमें +3 ऑक्सीकरण अवस्था सबसे अधिक सामान्य है। इसका कारण 4f, 5d तथा 6s उपकोशों के बीच अधिक ऊर्जा-अन्तर होना है। दूसरी ओर ऐक्टिंनाइड अधिक संख्या में ऑक्सीकरण अवस्थाएँ प्रदर्शित करते हैं क्योंकि 5f,6d तथा 7s उपकोशों में ऊर्जा-अन्तर कम होता है।
3. रासायनिक अभिक्रियाशीलता (Chemical reactivity) – लैन्थेनाइड (Lanthanides) सामान्य रूप से श्रेणी के आरम्भ वाले सदस्य अपने रासायनिक व्यवहार में कैल्सियम की तरह बहुत क्रियाशील होते हैं, परन्तु बढ़ते परमाणु क्रमांक के साथ ये ऐलुमिनियम की तरह व्यवहार करते हैं।
अर्द्ध- अभिक्रिया Ln3+ (aq) + 3e– → Ln(*) के लिए E– का मान -2.2 V से -2.4 V के परास में है। Eu के लिए E– का मान -2.0 V है। निस्सन्देह मान में थोड़ा-सा परिवर्तन है। हाइड्रोजन गैस के वातावरण में मन्द गति से गर्म करने पर ये धातुएँ हाइड्रोजन से संयोग कर लेती हैं। इन धातुओं को कार्बन के साथ गर्म करने पर कार्बाइड- Ln3C, Ln2C3 तथा LnC2 बनते हैं। ये तनु अम्लों से हाइड्रोजन गैस मुक्त करती हैं तथा हैलोजेन के वातावरण में जलने पर हैलाइड बनाती हैं। ये ऑक्साइड M2O3 तथा हाइड्रॉक्साइड M(OH)3 बनाती हैं। हाइड्रॉक्साइड निश्चित यौगिक हैं न कि केवल हाइड्रेटेड (जलयोजित) ऑक्साइड। ये क्षारीय मृदा धातुओं के ऑक्साइड तथा हाइड्रॉक्साइड की भाँति क्षारकीय होते हैं। इनकी सामान्य अभिक्रियाएँ चित्र-3 में प्रदर्शित की गई हैं।
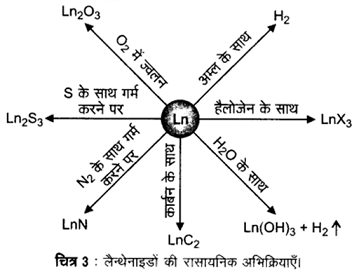
ऐक्टिनाइड (Actinides) – ऐक्टिनाइड अत्यधिक अभिक्रियाशील धातुएँ हैं, विशेषकर जब वे सूक्ष्मविभाजित हों। इन पर उबलते हुए जल की क्रिया से ऑक्साइड तथा हाइड्राइड का मिश्रण प्राप्त होता है और अधिकांश अधातुओं से संयोजन सामान्य ताप पर होता है। हाइड्रोक्लोरिक अम्ल सभी धातुओं को प्रभावित करता है, परन्तु अधिकतर धातुएँ नाइट्रिक अम्ल द्वारा अल्प प्रभावित होती हैं, इसका कारण यह है कि इन धातुओं पर ऑक्साइड की संरक्षी सतह बन जाती है। क्षारों का इन धातुओं पर कोई प्रभाव नहीं पड़ता।